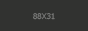Как сделать химическую грелку своими руками

В походе, на рыбалке, особенно в непогоду часто возникает нужда в обыкновенной грелке.
В походе, на рыбалке, особенно в непогоду часто возникает нужда в обыкновенной грелке. Конечно, неплоха и обычная резиновая, но у нее есть один существенный недостаток: очень уж медленно греется для нее на костре вода. Попробуем сделать химическую грелку. Для этого нам понадобятся самые обычные реактивы.
В походе, на рыбалке, особенно в непогоду часто возникает нужда обыкновенной грелке. Конечно, неплоха и обычная резиновая, но у нее есть один существенный недостаток: очень уж медленно греется для нее на костре вода.
Попробуем сделать химическую грелку. Для этого нам понадобятся самые обычные реактивы.
Для начала проведем несложный опыт. Пойдите на кухню и возьмите пачку поваренной соли. Впрочем, пачка не понадобится. Достаточно будет 20 г (2 чайных ложки). Затем загляните в шкафчик, где хранятся всевозможные хозяйственные препараты и материалы. Наверняка там сохранилось после ремонта квартиры немного медного купороса. Его понадобится 40 г (3 чайных ложки). Древесные опилки и кусок алюминиевой проволоки, надо полагать, тоже найдутся. Если так, все готово. Разотрите в ступке купорос и соль так, чтобы величина кристаллов не превышала 1мм (разумеется, на глаз). В полученную смесь добавьте 30 г (5 столовых ложек) древесных опилок и тщательно перемешайте. Кусок проволоки согните спиралью или змейкой, вложите в банку из-под майонеза. Туда же засыпьте подготовленную смесь так, чтобы уровень засыпки был на 1-1.5 см ниже горлышка банки. Грелка у вас в руках. Чтобы привести ее в действие, достаточно влить в банку 50 мл (четверть стакана) воды. Спустя 3-4 минуты температура грелки поднимется до 50-60° С.
Откуда берется в банке тепло, и какую роль играет каждый из компонентов? Обратимся к уравнению реакции:
CuSO4+2NaCl > Na2SO4+CuCl2
В результате взаимодействия медного купороса с поваренной солью образуется сульфат натрия и хлорная медь. Именно она нас интересует. Если вычислить тепловой баланс реакции, то окажется, что при образовании одной грамм-молекулы хлорной меди выделяется 4700 калорий тепла. Плюс теплота растворения в исходных образующихся препаратов — 24999 калорий. Итого: примерно 29600 калорий.
Тотчас же после образования хлорная медь вступает во взаимодействие с алюминиевой проволокой:
2Al+3CuCl2 > 2AlCl3+3Cu
При этом выделяется (также в пересчете на 1 г-моль хлорной меди) примерно 84000 калорий.
Как видите, в результате процесса суммарное количество выделяющегося тепла превышает 100000 калорий на каждую грамм-молекулу вещества. Так что никакой ошибки или обмана нет: грелка самая настоящая.
А что же опилки? Не принимая никакого участия в химических реакциях, они в то же время играют очень важную роль. Жадно впитывая в себя воду, опилки замедляют течение реакций, растягивают работу грелки во времени. К тому же древесина обладает достаточно низкой теплопроводностью: она как бы аккумулирует выделяющееся тепло и затем постоянно отдает его. В плотно закрытой посуде тепло сохраняется, по меньшей мере, два часа.
И последнее замечание: банка, конечно, не лучший сосуд для грелки. Она понадобилась нам только для демонстрации. Так что сами подумайте над формой и материалом для резервуара, в который поместить греющую смесь.
Источник: журнал "Юный техник", №5, 1983г., стр.78-79.